NSTEMI guideline – Összefoglaló
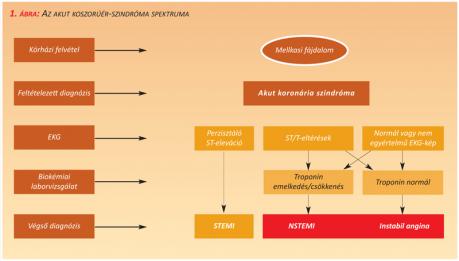
2012-01-24A kardiovaszkuláris kórképek közül a koszorúér-betegségek (CAD) esetében a legkedvezőtlenebbek a morbiditási és mortalitási mutatók. A CAD klinikai szempontból jelentkezhet néma (silent) iszkémia, stabil vagy instabil angina pectoris, miokardiális infarktus, szívelégtelenség vagy hirtelen szívhalál formájában. Általánosan elfogadott, hogy patofiziológiai szempontból ateroszklerotikus plakk ruptúrája, eróziója, majd erre rárakódó thrombus, esetleg disztális embólia által okozott myocardium perfúziós zavar áll a háttérben. E potenciálisan életet veszélyeztető állapot diagnózisának legelső és egyik legfontosabb klinikai tünete a mellkasi fájdalom. Az ESC (Európai Kardiológus Társaság) itt ismertetésre kerülő ajánlása az akut koszorúér-szindrómák (ACS) azon formáival foglalkozik, amelyekben a mellkasi fájdalmat nem kíséri perzisztáló ST-szakasz-eleváció EKG-jele (NSTE-ACS). A miokardiális nekroenzimek (troponin) szintjének emelkedésétől függ, hogy a diagnózis végül instabil angina (UAP) vagy non-ST-elevációs miokardiális infarktus (NSTEMI) lesz (1. ábra).
A kardiális troponinszint központi szerepet tölt be a diagnózis felállításában és a kockázat felmérésében, sokkal specifikusabb, mint a CK-MB és a mioglobin. MI esetén a tünetek kezdete után kb. 4 órával emelkedik meg a vérszintje és kb. 2 hétig marad a normál értéktartomány fölött. Sem diagnosztikus, sem pedig prognosztikai szempontból nincs lényeges különbség a troponin-T és -I között.
A non-invazív képalkotó eljárások közül az akut kivizsgálás során az echokardiográfia a legfontosabb eszköz. A bal kamrai szisztolés funkció meghatározása igen fontos prognosztikai értékű koszorúér-betegségben. Emellett az echokardiográfia lehetőséget ad az átmeneti falmozgászavarok (hipo- vagy akinézia) felismerésére, így hozzájárulhat a diagnózis megerősítéséhez, továbbá differenciáldiagnosztikai szempontból is értékes az aorta disszekciótól, pulmonalis embóliától, aortasztenózistól vagy hipertrófiás cardiomyopathiától való elkülönítés szempontjából.
A kardiális MR (CMR) vizsgálattal a funkció és a perfúzió együttes megítélése lehetséges, a hegszövet is detektálható, azonban ez az eljárás még nem széles körben elérhető, ami elmondható a multidetektoros CT-vizsgálat esetében is. Ez utóbbit jelenleg nem alkalmazzák az iszkémia kimutatására, annak ellenére, hogy a koszorúerek igen nagy felbontású, közvetlen megjelenítésére alkalmas.
Az invazív képalkotó eljárások közül a koronarográfia számít jelenleg is az arany standardnak a koszorúér-betegség megléte és súlyossága megállapításában. Ajánlatos intrakoronáriális nitrát adása előtt és után is elvégezni a vazokonstrikciós hatás kivédése és a dinamikus komponens ellensúlyozása céljából. Súlyos hemodinamikai instabilitás esetében megfontolandó intraaortikus ballonpumpa behelyezése a koronarográfia elvégzése előtt.
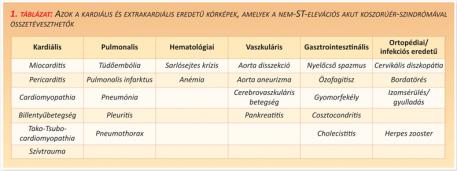
A differenciáldiagnosztikai szempontból szóba jöhető kórképeket az 1. táblázat foglalja össze (1. táblázat).
Diagnosztikai és terápiás lépések
Az ESC Guideline külön fejezetben foglalkozik azokkal a diagnosztikai és terápiás lépésekkel, szempontokkal, amelyek meghatározóak az NSTE-ACS klinikuma szempontjából. Az ajánlás a klinikai gyakorlat számára kitűnően alkalmazható egymást követő lépések sorozatában foglalta össze a lényeget, amit az alábbiakban mi is ismertetünk. Fontos azonban hozzátenni, hogy bizonyos speciális esetekben, egyes betegeknél eltérő lehet a stratégia, és egyedi mérlegelést igényel.
Első lépés: a kezdeti értékelés
NSTE-ACS gyanúja esetén a beteget azonnal kórházba kell küldeni, ahol erre specializálódott koronária őrzőben kezdődik meg az adekvát akut ellátás. Első lépésként a diagnózis késedelem nélküli felállítása a feladat az alábbi szempontok alapján:
- a mellkasi fájdalom milyensége – tünetközpontú fizikális vizsgálat;
- koszorúér-betegség valószínűségének felmérése (pl. kor, rizikófaktorok, anamnesztikus MI, CABG, PCI);
- EKG (ST-eltérés vagy egyéb abnormalitás észlelése).
Fentiek alapján, az első találkozástól számított 10 percen belül a beteg az alábbi 3 diagnosztikus kategória egyikébe sorolandó:
- STEMI;
- NSTE-ACS;
- ACS diagnózisa (igen) valószínűtlen.
A kórházba érkezéskor rögtön vérvétel (troponin-T vagy -I, kreatinin, hemoglobin, vércukor, vérsejtszám, standard biokémia) szükséges, hogy az eredmény 60 percen belül, az alább részletezett második lépéshez meglegyen.
Második lépés: diagnózis megerősítése és kockázatfelmérés
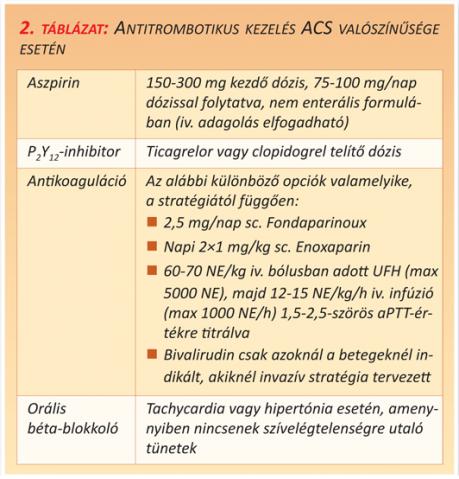
Miután a beteg az NSTE-ACS diagnosztikus csoportba került, a 2. táblázatban részletezetteknek megfelelően intravénás és orális antitrombotikus kezelést kell indítani (2. táblázat). A további kezelést a következők alapján kell meghatározni:
- Hogyan reagál a beteg az antianginás kezelésre?
- Milyenek a vérvizsgálati eredmények? (Különös tekintettel a troponinokra felvételkor, illetve 6-9 óra elteltével, a klinikai kémiára, a D-dimerekre, BNP NT-proBNP-értékekre.)
- Hogyan változik a megismételt EKG vagy folyamatos EKG-monitorozás során az ST-szakasz?
- Milyen az iszkémiás kockázati (Grace) score?
- Milyen az echokardiográfiás lelet?
- Milyen a mellkasröntgen-kép, CT vagy MR-eredmény? (Differenciáldiagnosztikai szempontból aorta disszekciótól vagy tüdőembóliától történő megkülönböztetés céljából.)
- Milyen a vérzéses kockázat (CRUSADE score)?
A személyre szabott kezelés függ a prognózistól (rizikófaktorok), ami a vérkémiai paraméterek, valamint a képalkotó eljárások által készült leletek alapján határozható meg pontosan. A kockázatfelmérés fontossága óriási, és folyamatosan újra kell értékelni. Magában foglalja mind az iszkémiás, mind pedig a vérzéses kockázatot. Az adekvát farmakológiai megoldás (kettős vagy hármas trombocitaaggregáció-gátlás, antikoagulálás, dózisok) megválasztásának kulcsszerep jut. Különös figyelmet kell fordítani a vesefunkció-zavarra, ami meglehetősen gyakori idős és/vagy diabéteszes betegeknél.
Harmadik lépés: invazív stratégia
A szívkatéterezést követő revaszkularizációról kimutatták, hogy segít a visszatérő iszkémia megelőzésében, javítja mind a rövid mind a hosszú távú prognózist. Számos rizikófaktor (troponin-emelkedés, diabétesz, ST-depresszió, veseelégtelenség) megléte esetében igazolt az invazív beavatkozás egyértelmű előnye. A kockázat időfaktorától függően az angiográfia elvégzése az alábbi négy kategória szerint történhet:
- invazív (<72 óra),
- sürgős invazív (120 perc),
- korai invazív (<24 óra),
- elsődlegesen konzervatív.
Sürgős invazív stratégia (<120 perccel az első orvosi észlelést követően).
Nagyon nagy kockázatú betegek esetében alkalmazandó, úgymint:
- refrakter angina (kialakuló MI ST-eltérés nélkül),
- intenzív antianginás kezelés ellenére visszatérő angina (2 mm-es), ST-depresszióval, vagy mély, negatív T-hullámokkal,
- szívelégtelenség klinikai tünetei, vagy hemodinamikai instabilitás (sokk),
- életet veszélyeztető aritmiák (kamrafibrilláció vagy kamrai tachycardia).
GP IIb/IIIa-receptor-gátló (eptifibatid vagy tirofiban) adása megfontolandó ilyen esetekben. Kórházi hazabocsátás előtt terheléses vizsgálat végzése ajánlatos a további kezelés meghatározása szempontjából és elengedhetetlen az elektív angiográfia indikációjához.
Negyedik lépés: a revaszkularizáció formái
Ha az angiográfiás kép ateromatózus elváltozást mutat kritikus koronárialézió nélkül, a beteg számára konzervatív gyógyszeres kezelés javallt. Újra kell értékelni az NSTEMI ACS diagnózisát és különös figyelmet kell fordítani a fennálló tünetek hátterében álló esetlegesen más etiológiai tényező felderítésére, mielőtt a beteget hazaengedjük a kórházból. A kritikus koszorúér-léziók hiánya azonban nem zárja ki a diagnózist, ha a mellkasi fájdalom tipikus volt, és a biomarker-értékek pozitívak. Ilyen esetekben az ajánlott kezelés az NSTE-ACS-terápia.
A választandó revaszkularizációs eljárás NSTE-ACS esetében megegyezik az elektív revaszkularizációhoz adott ajánlásban rögzítettekkel. Egyér-betegség esetén a „culprit” lézióban PCI elvégzése javasolt stent-beültetéssel, mint elsőként választandó beavatkozás. Többér-betegség esetén egyedi mérlegelés szükséges annak eldöntésére, hogy PCI vagy CABG a választandó beavatkozás. Szekvenciális megközelítés szükséges, azaz először PCI a „culprit” lézióban, amit elektív CABG követhet más, a culprit lézión kívüli, károsodott koronária régió(k)ban igazolt iszkémia vagy funkcionális károsodás (FFR) bizonyítéka esetén.
PCI során nem kell változtatni az antikoaguláns gyógyszert. Fondaparinoux kezelés esetén UFH adása javallt a PCI elvégzése előtt. GP IIb/IIIa-inhibitor adása jön szóba troponinszint-emelkedéskor, vagy thrombus angiográfiás bizonyítéka esetén. CABG tervezésekor a P2Y12-inhibitorok adását fel kell függeszteni, és a műtétet csak akkor szabad elkezdeni, ha az a klinikai tünetek és az angiográfiás lelet alapján indokolt.
Amennyiben angiográfiával nem támasztható alá a revaszkularizáció szükségessége, nincs nyugalmi angina, mert intenzív gyógyszeres kezeléssel a beteg tünetmentessé vált, másodlagos, a prevencióra irányuló lépések szükségesek (1. ábra).
Ötödik lépés: kórházi elbocsátás és az azt követő kezelés/gondozás
Igaz ugyan, hogy NSTE-ACS diagnózisa esetén a legtöbb adverz esemény a korai szakban következik be, azonban az MI vagy hirtelen szívhalál kockázata ezeknél a betegeknél továbbra is, (akár még több hónapig) magasabb marad. Korai revaszkularizáció utáni betegek esetében viszonylag alacsony (2,5%) az életet veszélyeztető aritmiák kockázata, amely 80%-os valószínűséggel a tünetek kezdetétől számított 12 órán belül következik be.
Mindezek értelmében a tünetek kezdete utáni 24-48 órával történő monitorozás rutinszerű alkalmazásának szükségessége nem bizonyított. Az NSTE-ACS diagnózisú betegeket legalább 24 óráig kórházi megfigyelés alatt kell tartani, amennyiben a „culprit” léziót stent-implantációval sikeresen megoldották.
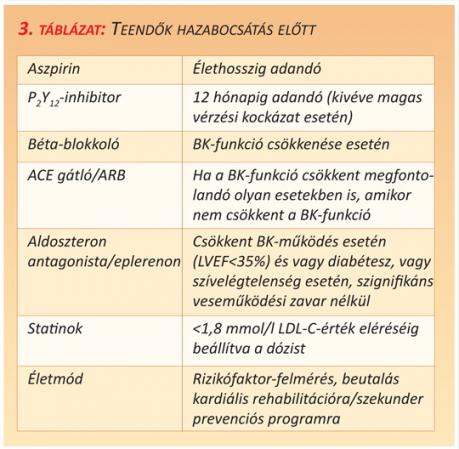
Szükséges azonban az intenzív rizikófaktor felmérés és a kockázati tényezők folyamatos újraértékelése, minden beteget ellátva életmód-változtatási és életviteli tanácsadással. A hazabocsátás után ajánlatos a beteget kardiális rehabilitációs programba bevonni, ami egyrészt javítja a gyógyszeres kezeléssel kapcsolatos „compliance” értékét, másrészt segít a rizikófaktorok csökkentésében. A kórházi elbocsátáskor elvégzendő teendők listáját a 3. táblázatban foglaltuk össze (3. táblázat).
Forrás:
Hamm CW, Bassand JP, et al. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. European Heart Journal 2011; doi:10.1093/eurheartj/ehr236
Cikk értékelése
| Eddig 17 felhasználó értékelte a cikket. |

Hozzászólások